Разработването на лекарства е високорисково и продължително. Изчакването за потенциални нови лечения е трудно за пациентите, особено тези с редки или трудни за лечение състояния, и ако пазарът е малък, цената на одобреното лекарство може да бъде висока. Преназначаването и препозиционирането на съществуващи лекарства (известно още като препрофилиране) може да ускори процеса и да намали необходимите финансови инвестиции в сравнение с новите лекарства, като гарантира, че пациентите могат да получат достъп до лечение по-бързо и на по-достъпни цени.[1, 2]
Има четири ключови групи преназначени лекарства – предлагани на пазара лекарства със съществуващи или изтекли патенти, лекарства, които са прекратени на клинични или регулаторни етапи, стереоизомери или метаболити на съществуващи лекарства или кандидати, при които са направени незначителни промени в съществуващи лекарства. Важно е да запомните, че неуспехът на лекарството в клиничните изпитвания не е причинен само от проблеми с ефикасността или безопасността – това може да се дължи на промяна на посоката на действие на компанията, проблеми с формулировката или защото има проблеми с търговски интерес или лошо стратегическо планиране.[3]
Ползите от пренасочването и препозиционирането на лекарства
Въпреки че двата термина често се използват взаимозаменяемо, повторното използване на лекарства може да се отнася до приемане на одобрено лекарство и използването му за друго показание. Препозиционирането на лекарството може да се отнася до рестартиране на разработката на лекарство, което е спряло, за да се получи одобрение за ново показание.[1]
Основните ползи от преназначаването или препозиционирането на лекарствата са свързани с разходите и времето. Времевата рамка за разработване на преназначено лекарство обикновено е от една до три години, в сравнение със средно 12 години за ново лекарство.[4]
За компания, разработваща лекарство, чието развитие е спряло, или такова, което е достигнало пазара за друго показание, възможността за „рециклиране“ на съществуващите предклинични и/или клинични данни за безопасност, токсичност и фармакокинетика/фармакодинамика ще спести пари и време . Освен това им позволява да възстановят парите, инвестирани в това, което иначе би могло да бъде неуспешно лекарство. Съществуващите знания също намаляват риска от провал.
Лекарства, които са се провалили или се провалят в разработването, но все още имат известна патентна защита, могат да бъдат препозиционирани за друго показание от компанията-оригинатор или лицензополучател. Преназначаването може също така да позволи на компаниите да удължат жизнения цикъл на собствените си предлагани на пазара лекарства, които наближават изтичането на патента, тъй като могат да получат защита за новото показание. Пренасочването и препозиционирането на лекарства също може да бъде ценно за компаниите, разработващи лекарства за редки заболявания, като насърчава сътрудничеството и споделянето на данни и ресурси.[3, 5]
Стъпките за разработване и получаване на одобрение за повторно предназначено лекарство могат да включват:
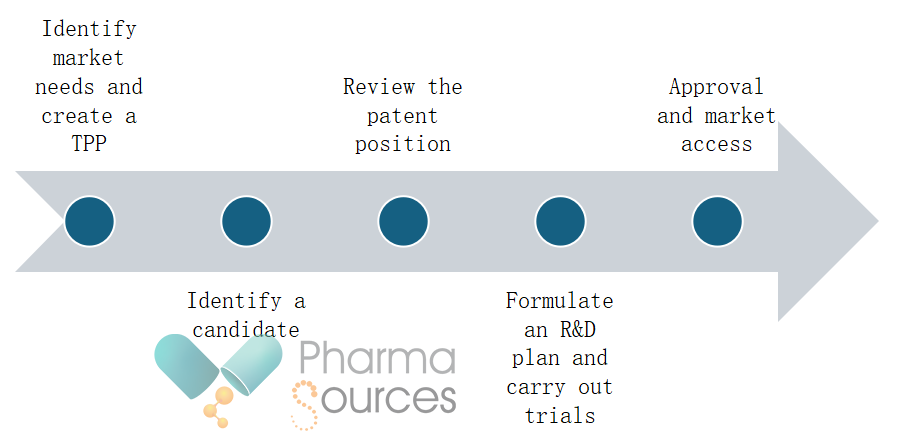
Идентифицирайте нуждите на пазара и създайте целеви продуктов профил
За компания, която иска да пренасочи лекарство, но няма предвид съществуващ кандидат, първата стъпка е да оцени пазарния пейзаж, за да види дали има нужда от ново лекарство на пациента и дали компанията ще може да се възстанови инвестициите в разработването на лекарства. Това се поддържа чрез разработване на целеви продуктов профил (TPP). TPP описва желаните характеристики на лекарство в процес на разработка за конкретно заболяване. Той предоставя на компанията ръководство по време на разработването на лекарства за всички участващи екипи. [2, 6, 7]
Областите, обхванати от TPP, които също са полезни за преглед, когато една компания има предвид конкретен кандидат, включват:[2, 7, 8]
●Индикация
○ Индикация за първоначална цел
○Потенциални бъдещи индикации
●Население
○ Първоначален целеви пазар – икономически приоритети или области с най-голяма незадоволена нужда
○ Проучване на осъществимостта
○ Изискване за придружаваща диагностика за идентифициране на субпопулации
●Насочване/фармакокинетика
●Безопасност, поносимост и ефикасност
○Крайни точки на изследването
○Предимства в сравнение с настоящи/бъдещи конкуренти или стандарт на грижа
●Взаимодействия лекарство-лекарство
●Стабилност
○Изисквания за съхранение
○ Може да зависи от целевите пазари
●Път на приложение/формулиране
○Текуща формулировка/потенциал за преформулиране
○Кой начин на приложение ще бъде предпочетен от пациентите?
○ Ще се изисква ли устройство за доставка и дали вече е налично
●Честота на дозиране
○Разгледайте в сравнение със стандарта на грижа
●Цена
○Целева цена на доза, базирана на анализ на конкурентния ландшафт
●Време до наличност
○Време, необходимо за клинични изпитвания и регулаторни процеси
○Време, необходимо за оценки на здравни технологии (HTA)
Идентифицирайте кандидат
Една компания може да има предвид лекарство като кандидат за пренасочване, например базирайки ново показание на констатация, разглеждана като страничен ефект в предишен процес на разработка.

За компания, която търси лекарство за конкретна цел или индикация, подходите могат да бъдат целеви, структурни, сигнатурни, пътеки, мрежови, знания или клинични данни, като специфичните подходи включват:[13-17]
● Менделска рандомизация за установяване на връзки между фенотипове и генетично предвидени лекарствени ефекти
● Мащабни мултиомични данни за по-добро разбиране на етиологията на заболяването и идентифициране на нови лекарствени цели
● Машинно обучение за идентифициране на подтипове болести и лекарствени цели или за свързване на патология и молекулярни механизми
● Генеративен AI или интегриране на експресия на човешки ген, лекарствени смущения и клинични данни за идентифициране на кандидати
Прегледайте патентната позиция
Компания, която иска да пренасочи или препозиционира лекарство, трябва да е наясно със съществуващата патентна позиция, включително патенти за оригиналното съединение и за формулировки, режими на дозиране или специфични употреби. Ако лекарството все още е покрито от патент, тогава те ще трябва да се свържат с притежателя на патента и да видят дали се интересуват от сътрудничество или лицензиране на лекарството. Ако лекарството е без патент, има по-голяма свобода за работа.[4]
Всички лекарства, включително преназначени и препозиционирани лекарства, се нуждаят от ниво на патентна защита, за да се позволи на преназначената компания да възстанови разходите си, преди да се сблъска с конкуренция. Новите видове патенти могат да включват: [4, 18]
●Терапевтична индикация
●Формулация
●Дозов режим
● Система за доставка
● Комбинация от лекарства
●Комбинация лекарство/изделие
Формулирайте план за научноизследователска и развойна дейност и провеждайте опити
За да разработят успешно преназначено лекарство, компаниите трябва да работят с клиницисти и мултидисциплинарен екип от вътрешни и външни експерти, които да подкрепят процеса на разработка. Преназначените лекарства все още трябва да имат достатъчно предклинични данни, да преминат през клинични изпитвания и да отговарят на строги регулаторни стандарти в новото си показание. Въпреки че съществуващите данни при хора и не при хора ще подкрепят безопасността и токсичността, ще са необходими допълнителни клинични проучвания, за да се потвърди ефикасността при целевата група пациенти, преди да бъдат представени за одобрение.[8]Работата с пациенти и групи за застъпничество на пациентите също е важна, за да разберат от какво се нуждаят от лечението и да наемат участници за клинични изпитвания.[4]
Одобрение и достъп до пазара
Тясното сътрудничество с регулаторните органи и органите за оценка на здравни технологии (HTA) ще подпомогне ефективен процес към одобрение, предлагане на пазара и възстановяване на разходи. Регулаторните органи могат да посъветват какви клинични изпитвания ще са необходими и да предложат кой път за одобрение, включително ускорените пътища, ще бъде най-подходящ за конкретно лекарство и показание.[4]
В обобщение
Пренасочването и препозиционирането на лекарства предлага рентабилен и ефективен път към пазара, който позволява на пациентите да получат по-бърз достъп до лекарства. Компаниите трябва да са сигурни, че събират правилните данни за гладък процес и това може да бъде подпомогнато чрез сътрудничество с пациенти, други компании, регулаторни органи и органи за оценка на здравни технологии.
Референции
1. Bakker, A., Привидно малък семантичен проблем е основна пречка пред разработването на лечения за редки заболявания. STAT, 2023 г. Достъпно от: https://www.statnews.com/2023/06/27/drug-repurposing-repositioning-rare-diseases/.
2. Griffiths, A., et al., Профили на целеви продукти във фармацевтичното развитие KPMG. 2023. Достъпно от: https://assets.kpmg.com/content/dam/kpmg/uk/pdf/2023/01/target-product-profiles-in-pharmaceutical-development.pdf.
3. Елвидж, С., Изваждане на препозициониращия джин джин от бутилката. Life Science Leader, 2010. Достъпен от: https://www.lifescienceleader.com/doc/getting-the-drug-repositioning-genie-out-of-the-bottle-0001.
4. Pisani, J., et al., Повторно използване на лекарства: възможността и предизвикателството. 2021. Достъпно от: https://www.lifearc.org/wp-content/uploads/2024/03/RD-Drug-repurposing-report.pdf.
5. Тейлър, М., М. Салова и А. Шрьодер, Преназначение на лекарства: Потенциал за разширяване на лечението на редки болести. Avalere: Прозрения и анализ, 19 февруари 2024 г. Достъпен от: https://avalere.com/insights/drug-repurposing-potential-to-expand-rare-disease-treatment.
6. Щатен писател. Насочете продуктови профили. Световна здравна организация. 9 юли 2024 г. Достъпно от: https://www.who.int/observatories/global-observatory-on-health-research-and-development/analyses-and-syntheses/target-product-profile/who-target-product -профили.
7. Щатен писател. Повторно предназначение на лекарство: ключови съображения. UCL Therapeutic Innovation Networks - UCL – University College London. 9 юли 2024 г. Достъпно от: https://www.ucl.ac.uk/ion/translation-enterprise/tailored-support-translational-researchers/re-purposing-drug/repurposing-drug.
8. Щатен писател. Repurposing Medicines Toolkit – Ръководство за навигация в процеса. LifeArc/Съвет за медицински изследвания. 11 юли 2024 г. Достъпно от: https://www.repurposingmedicines.org.uk.
9. Кръгла маса за превеждане на геномно-базирани изследвания за здравеопазване, Съвет по политика в областта на здравните науки и Институт по медицина, в преназначаване и препозициониране на лекарства: Резюме на семинара. 2014: Вашингтон (окръг Колумбия).
10. Ghofrani, HA, IH Osterloh и F. Grimminger, Sildenafil: от стенокардия до еректилна дисфункция до белодробна хипертония и отвъд. Nat Rev Drug Discov, 2006. 5(8): p. 689-702.
11. Gohel, D., et al., Силденафил като кандидат лекарство за болестта на Алцхаймер: Наблюдение на данни за пациенти в реалния свят и механични наблюдения от индуцирани от пациента плурипотентни неврони, получени от стволови клетки. J Alzheimers Dis, 2024. 98 (2): p. 643-657.
12. Dorset Medicines Advisory Group, НАСОКИ ЗА СПОДЕЛЕНА ГРИЖА ЗА СИЛДЕНАФИЛ ЗА ЛЕЧЕНИЕ НА ВТОРИЧЕН ФЕНОМЕН НА РЕЙНО, СВЪРЗАН СЪС СИСТЕМНА СКЛЕРОЗА NHA. 2017. Достъпно от: https://nhsdorset.nhs.uk/Downloads/aboutus/medicines-management/Shared%20Care%20Guidelines/Sildenafil%20Shared%20Care%20Documented%20July%2017.pdf.
13. Wang, L., et al., Пейзажът на методологията при повторно използване на лекарства с помощта на човешки геномни данни: систематичен преглед. Кратка биоинформация, 2024. 25 (2).
14. Sperry, M. и DE Ingber, Стратегии за пренасочване на лекарства, предизвикателства и успехи. 4 март 2024 г. Достъпно от: https://www.technologynetworks.com/drug-discovery/articles/drug-repurposing-strategies-challenges-and-successes-384263#D3.
15. Rodriguez, S., et al., Машинното обучение идентифицира кандидати за повторно използване на лекарства при болестта на Алцхаймер. Nat Commun, 2021. 12 (1): стр. 1033.
16. Yan, C., et al., Използване на генеративен AI за приоритизиране на кандидатите за повторно използване на лекарства за болестта на Алцхаймер с клинично валидиране в реалния свят. NPJ Digit Med, 2024. 7(1): p. 46.
17. Wu, P., et al., Интегриране на генна експресия и клинични данни за идентифициране на кандидати за повторно използване на лекарства за хиперлипидемия и хипертония. Nat Commun, 2022. 13 (1): стр. 46.
18. Conour, J., Защо патентите за метод на лечение за повторно предназначени лекарства си заслужават инвестицията. JD Supra: Новини и прозрения, 5 октомври 2020 г. Достъпно от: https://www.jdsupra.com/legalnews/why-method-of-treatment-patents-for-92813/.

